

红花为菊科植物红花Carthamus tinctorius L.的干燥花,夏季花由黄变红时采摘,阴干或晒干。红花含有黄酮、查尔酮、生物碱等多种活性成分[1-3],是中药、藏药共有的大品种药材,但是中、藏医对其功效认识不尽相同。中医用其活血通经,散瘀止痛之效,现代研究也表明,红花中主要含有抗凝血、抗血小板形成等作用[2,4],主要用于治疗心脑血管疾病。而藏医《四部医典》记载其“封闭脉口,治疗一切肝病”,广泛应用于二十五味松石丸、七味铁屑丸等治疗肝病的藏成药中,因而被誉为保肝圣药。现代研究也表明,红花提取物具有保肝、抗肝纤维化的作用[2]。我国红花栽培历史悠久,主要产地为新疆、甘肃、河南、山东、四川等地[5]。西藏林芝地区位于我国青藏高原的西南部,海拔2500~3000m,是藏药材的主要产地,红花等藏药材种植历史悠久,但尚未有学者对青藏高原等高海拔地区种植的红花进行研究和报道。本课题采用《中国药典》(2010年版)“红花”项下的各项指标为标准,对该地区的红花质量进行研究。同时由于其他红花主产区环境污染,包括人为等因素所致环境中的重金属有害元素含量增加,会导致药材品质的降低,还有可能危害到人体健康,所以本文采用ICP-MS对该地区红花中的铅(Pb)、砷(As)、镉(Cd)、铬(Cr)、铍(Be)、铊(Tl)、碲(Te)、钕(Nd)等主要重金属进行了研究。项研究旨在为评价该地区红花中重金属有害元素含量及其药材质量提供一定科学依据,为促进当地藏药材合理使用和健康发展奠定基础。
1 材料
Agilent 7500ce型电感耦合等离子体质谱仪;LC-20AT高效液相色谱仪;Sartorius BP211D天平;Mars xpress微波消解仪;BHW-09C型加热板;Labtech H210 型循环冷却水泵。
铍(Be)、镉(Cd)、砷(As)、铊(Tl)、铬(Cr)、碲(Te)、钕(Nd)、铅(Pb)标准物质,均来自中国计量科学研究院。(批号分别为GSB 04-1718-2004,GBW08612 12106,GSB 04-1758-2004,GBW08614 13041,GBW(E)080117 12111,GBW(E)080548 11101,BW3134 1004,GBW08619 12062)国家一级标准物质杨树叶(地矿部物化探研究所GBW07604)P/A调谐液浓度(10% HNO3 介质,Agi-lent)。调谐液(2% HNO3介质,Agilent,批号5184-3566);羟基红花黄色素A对照品(中国食品药品检定研究院,批号111637-200502);山柰素对照品(中国食品药品检定研究院,批号110861-200405);硝酸BVIII级;甲醇、乙腈为色谱纯;磷酸为分析纯;蒸馏水与纯净水(实验室自制);各个批红花样品均自采于中国藏学研究中心西藏林芝藏药材种植实验基地,1批样品于采用新疆昌吉,后经内蒙古药检所周凯教授鉴定为红花C.tinctorius的干燥花。样品保存于中国藏学研究中心藏医药研究所。
2 方法与结果
2.1 重金属研究的方法与结果
2.1.1 仪器设定参数 RF功率为1200W,冷却气流量为20L·min-1,载气为1.08L·min-1,采样深度为7.5mm,蠕动泵快速提升速度为0.3r·s-1维持30s,蠕动泵分析前稳定转速为0.1r·s-1维持30s,数据采集时间约为3s。
2.1.2 内标溶液的制备 精密吸取钪(Sc)、钇(Y)、铟(In)、铋(Bi) 的单元素标准溶液适量,以1%硝酸逐级稀释成质量浓度为1mg·L-1的混合溶液,摇匀,即得。
2.1.3 标准溶液的配制 精密吸取8种待测元素的单元素标准溶液适量,用1%硝酸溶液逐步稀释成不同的浓度。以1%硝酸溶液作为标准空白溶液,见表1。
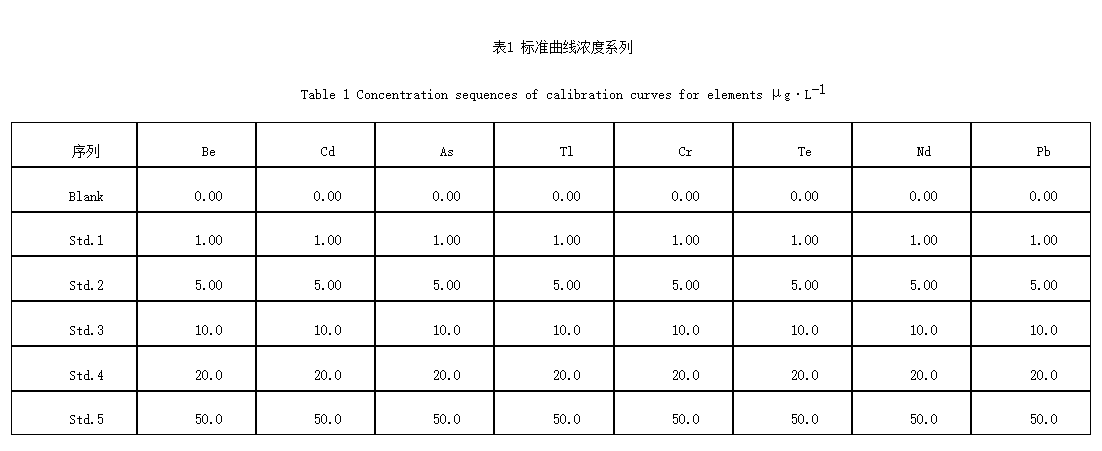
2.1.4 标准曲线及供试品测定 用定量分析方法对2.1.3项下配制的不同浓度标准溶液和2.1.6项下供试品溶液测定。测定时,仪器的内标管始终插在内标溶液中,依次将仪器的样品管插入各个浓度的标准溶液(包括空白溶液)中进行测定,以每一浓度3次读数的平均值为纵坐标,相应的浓度为横坐标作标准曲线。再将样品管插入供试品溶液进行测定。线性范围为0~50μg·L-1,见表2。
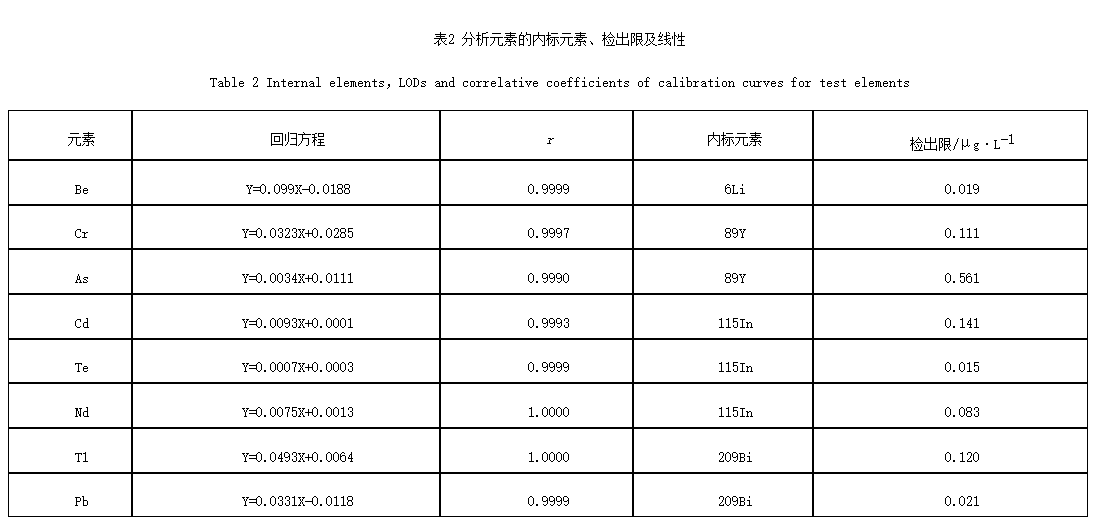
2.1.5 方法的检出限 方法的检出限和该方法所选用的空白溶液和试验操作中仪器设备有关。本方法以1%的硝酸溶液作为空白溶液。平行测定空白溶液11次,计算每种元素的标准偏差(R2),3R对应的浓度即为各元素的检出限,本方法中各元素检出限都在0.019~0.561μg·L-1。
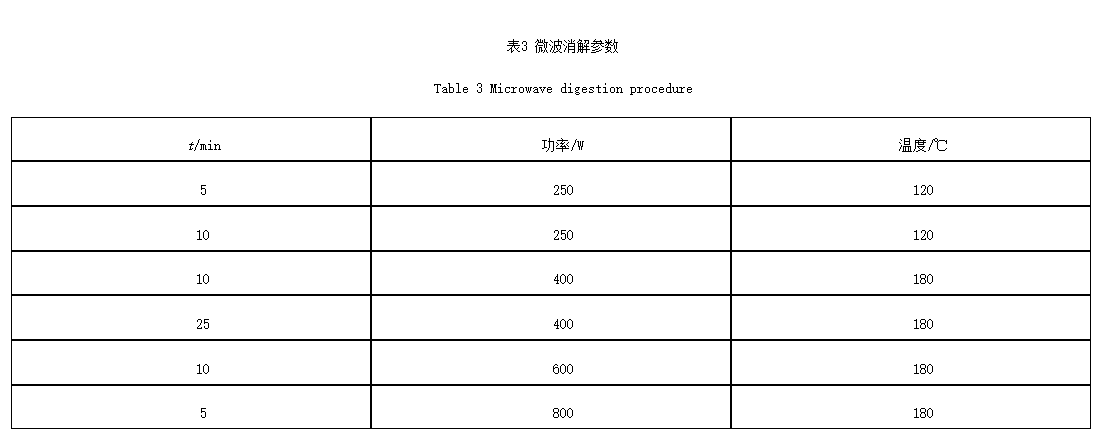
2.1.6 供试品制备 取本品0.1g,精密称定,置于聚四氟乙烯内管中,加8mL硝酸和2mL过氧化氢,放置2h后,置微波消解装置中消解,消解程序,见表3。而后冷却,用水将溶液转移至50mL聚四氟乙烯的量瓶中并定容至刻度,摇匀,供ICP-MS测定。
2.1.7 重复性试验 精密称取红花粉末0.1g,按2.1.6 项下的规定操作,平行实验5份,测定,计算各元素含量的平均值及RSD。各元素的RSD都小于10%,表明重复性良好。
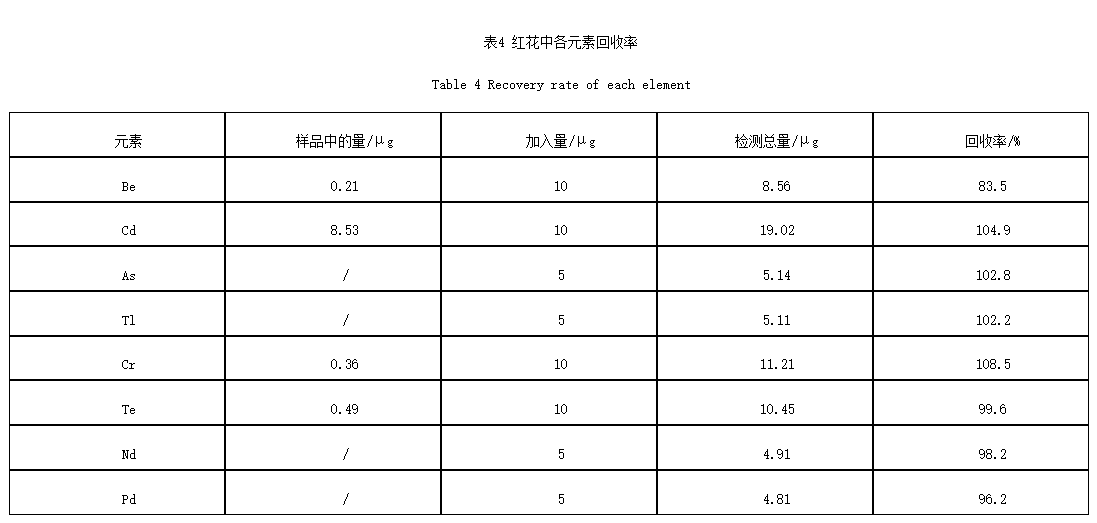
2.1.8 加样回收率试验 精密称取样品粉末(过4号筛)约0.1g于消解罐,并精密加入等量的各元素储备液适量,按2.1.6项下的规定操作,平行实验5份,测定,以加标前后测定的含量平均值计算各元素的回收率,见表4。各元素的回收率在83.6%~109.2%,能满足实验的要求。
2.1.9 随行标准物质测定 实验随行测定国家一级标准物质杨树叶,进一步论证方法的准确性。精密称取标准物质茶叶约0.10g,按2.1.6项下的规定操作,平行实验5份,测定,计算各元素含量的平均值及RSD均在标准值规定的范围内。
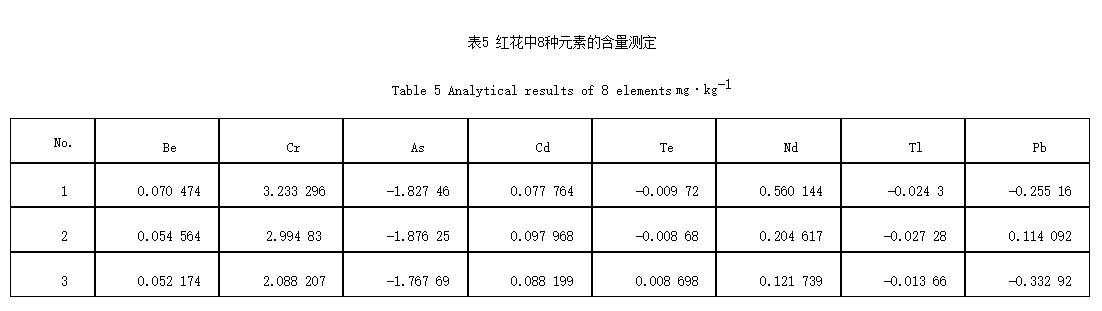
2.1.10 供试品分析 精密称取供试品0.10g,按2.1.6项下的规定操作,平行实验2份,测定,计算含量,见表5。
2.2 羟基红花黄色素A的测定[1]
2.2.1 色谱条件YMC C18色谱柱(4.6mm×250mm,5μm);流动相为甲醇-乙腈-0.7%磷酸水溶液(26∶2∶72);检测波长403nm;流速1.0mL·min-1;柱温30℃;进样量10μL。
2.2.2 对照品溶液的制备 取羟基红花黄色素A对照品适量,精密称定,加25%甲醇制成0.131g·L-1的溶液。
2.2.3 供试品溶液的制备 取本品粉末(过3号筛)0.40g,精密称定,置具塞锥形瓶中,精密加入25%甲醇50mL,称定质量,超声处理(功率300W,频率50kHz)40min,放冷,再称定质量,用25%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
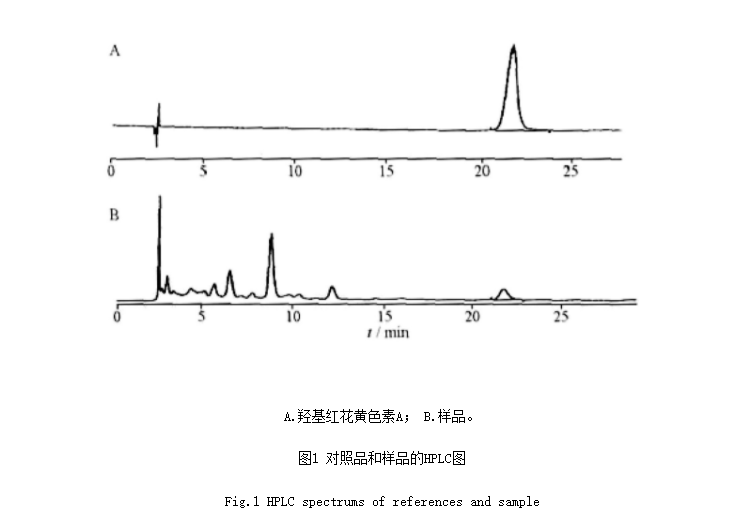
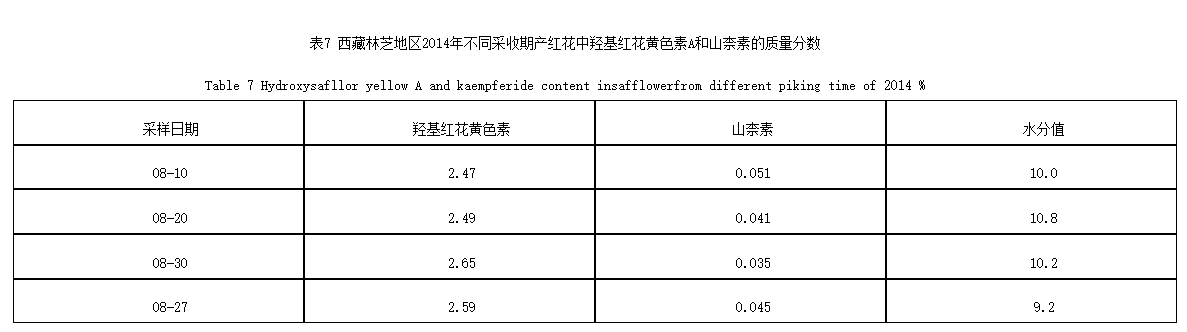
2.2.4 样品测定 分别精密吸取对照品溶液与供试品溶液各10μL,注入液相色谱仪,按上述方法进行测定,见图1。羟基红花黄色素A历年测定结果,见表6,2014年度不同采收期测定,见表7。

2.3 山柰素的测定[1]
2.3.1 色谱条件YMC C18色谱柱(4.6mm×250mm,5μm);流动相为甲醇-0.4%磷酸水溶液(52∶48);检测波长367nm;体积流量1.0mL·min-1;柱温30℃;进样量10μL。
2.3.2 对照品溶液的制备 取山柰素对照品适量,精密称定,加甲醇制成0.10g·L-1的溶液,即得。
2.3.3 供试品溶液的制备 取本品粉末(过3号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇25mL,称定质量,加热回流30min,放冷,再称定质量,用甲醇补足失重,摇匀,滤过,精密量取续滤液15mL,置平底烧瓶中,加盐酸溶液(15~37)5mL,摇匀,置水浴中加热水解30min,立即冷却,转移至25mL量瓶中,用甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
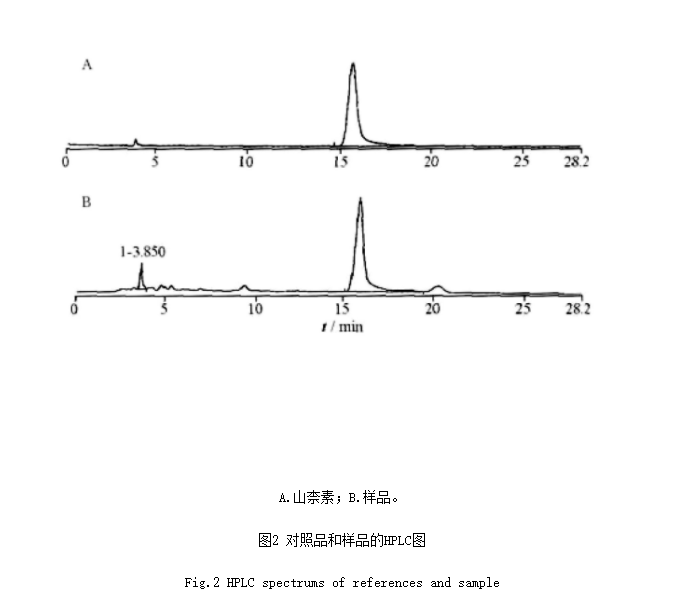
2.3.4 样品测定 分别精密吸取对照品溶液与供试品溶液各10μL,注入液相色谱仪,按上述方法进行测定,见图2。山柰素历年测定,见表6,2014年度不同采收期测定,见表7。
3 讨论
由各批红花中的重金属含量结果可知,该地区红花中所含的砷、铅重金属含量较少[11]。可能与该地区地处青藏高原,环境污染较少有关,为西藏林芝地区红花的作为优良产区提供一定科研数据。
通过红花样品中羟基红花黄色素A和山柰素的测定结果可知,该地区收集的红花样品,其羟基红花黄色素A和山柰素的含量均高于药典标准。
该产地红花2014年不同采收期数据推断,羟基红花黄色素A的含量受采收期影响较小;山柰素的含量受采收期影响较大,可作为最佳采摘季节提供依据。
——————————————————————
[参考文献]
[1]中国药典.一部[S].2010:157.
[2]Zhou X,Tang L,Wang Z,et al,Towards a better understanding of medicinal uses of Carthamus tinctorius L.in traditional Chinese medicine: a phytochemical and pharmacological review[J].J Ethnopharmacol,2014,151:27
[3]姜建双,夏鹏飞,冯子明,等.红花化学成分研究[J].中国中药杂志,2008,33(24):2911.
[4]陈梦,赵丕文,孙艳玲,等.红花及其主要成分的药理作用研究进展[J].环球中医药,2012,5(7):556.
[5]赵钢,王安虎.红花的资源及要用价值[J].中国野生植物资源,2004,23(3):761.
[6]温慧敏,陈晓辉,董婷霞,等.ICP-MS法测定4种中药材中重金属含量[J].中国中药杂志,2006,31(16):1314.
[7]王艳泽,王英锋,施燕支,等.微波消解ICP-MS法测定根和根茎类生药中11种微量元素[J].光谱学与光谱分析,2006,26(12):2326.
[8]邵幼岩,蔡碧双,林纪昀,等.ICP-MS测定13种糖尿病药膳常用中药中的微量元素[J].中国中药杂志,2007,32(19):2011.
[9]何平,孙巍,孙玉侠,等.微波消解-ICP-MS法测定丹参和三七药材中18种重金属元素[J].中成药,2011,33(12):2110.
[10]刘雅新,刘珊珊,谭勇,等.新疆不同产地红花质量评价[J].中成药,2014,36(1):141.
[11]宋玉龙,石明辉,贾盛杰,等.新疆不同产地红花中重金属及农药残留量分析[J].吉林中医药,2015,35(1):68.
版权所有 中国藏学研究中心。 保留所有权利。 京ICP备06045333号-1
京公网安备 11010502035580号



